Teva GmbH | Neues Packungsdesign
FRISCHER LOOK FÜR RATIOPHARM PRODUKTE
Seite 1/1 5 Minuten
„In den vergangenen Jahren haben wir viel erreicht: ratiopharm wird von den Apotheken als Partner geschätzt und die Kunden nehmen uns als eine starke Marke wahr, die ihnen hilft, sich innerhalb der Vielzahl der angebotenen Präparate zu orientieren. Darauf wollen wir aufbauen und die Marke weiter stärken. Daher haben wir das Produktdesign unserer bekanntesten Produkte modernisiert, um uns somit auch optisch noch mehr vom Wettbewerb abzuheben“, erläutert Anette Spieß, Projektmanagerin OTC bei ratiopharm. „Gleichzeitig war uns bei der Weiterentwicklung des Designs aber auch wichtig, dass für unsere Kunden der Wiedererkennungswert der ratiopharm Produkte erhalten bleibt und wir unserem bewährten Markenauftritt treu bleiben.“
Besser sichtbar in der Sichtwahl
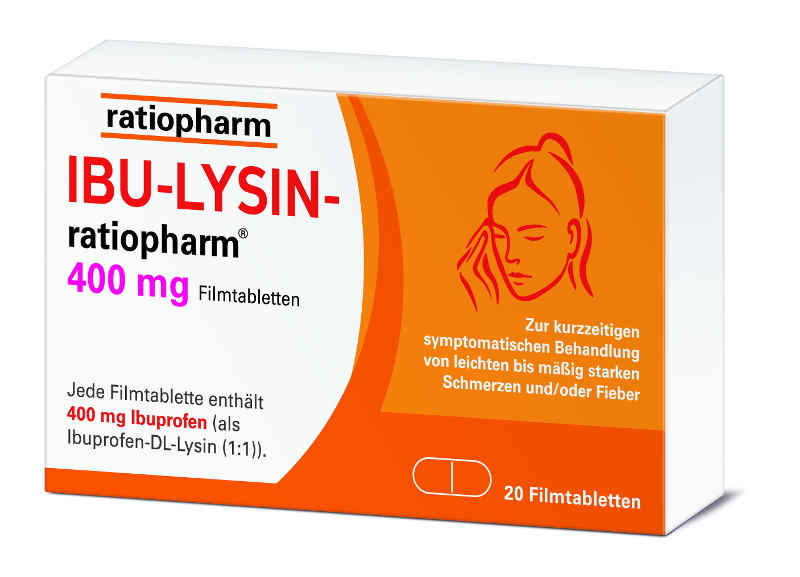
Das neue Design soll vor allem für höhere Aufmerksamkeit in der Sichtwahl sorgen: Dank einer neuen Schriftart wird die Lesbarkeit verbessert und der Produktname wird künftig farbig statt schwarz dargestellt. Zudem werden die bisherigen Schwarz-Weiß-Fotos auf der Verpackung durch moderne farbige Illustrationen ersetzt. Die runden, geschwungenen Elemente des Packungsdesigns transportieren die Dynamik der Marke.
„Kauf- und Verkaufsentscheidungen sind emotional geprägt – gerade im Apothekensegment, wo es um Gesundheit geht“, betont Anette Spieß. „Ein starkes Branding ist somit die Basis für eine gelungene Markenkommunikation.“
Umstellung erfolgt nach und nach
IBU-LYSIN-ratiopharm® 400 mg wird aktuell als erstes Produkt auf die neue Optik umgestellt, Ginkobil® ratiopharm und Vitamin B-Komplex-ratiopharm® werden noch in diesem Jahr folgen. Die 2021 gelaunchten Produkte Diclox forte 20 mg/g Gel und Paracetalgin 500 mg Filmtabletten sind bereits von Beginn an im modernisierten Design erhältlich.
IBU-LYSIN-ratiopharm® 400 mg Wirkstoff: Ibuprofen-DL-Lysin (1:1). Zusammensetzung: Jede Filmtbl. enth. 400 mg Ibuprofen (als Ibuprofen-dl-Lysin (1:1)). Sonst. Bestandt.: Tablettenkern: Mikrokristalline Cellulose, Croscarmellose-Natrium, Talkum, Hochdisperses Siliciumdioxid, Magnesiumstearat (Ph.Eur.) [pflanzlich]. Filmüberzug: Hypromellose, Macrogol 6000, Glycerol 85%. Anwendungsgebiete: Kurzzeitige symptomatische Behandl. von leichten bis mäßig starken Schmerzen wie Kopfschmerzen, Zahnschmerzen, Regelschmerzen sowie Fieber und Schmerzen bei Erkältungen. Kurzzeitige symptomatische Behandl. der akuten Kopfschmerzphase bei Migräne mit od. ohne Aura. Dieses AM wird bei Kdrn ab 20kg KG (ab 6J.), Jugendl. und Erw. angewendet. Gegenanzeigen: Überempfindlichkeit gg. den Wirkstoff Ibuprofen od. einen der sonst. Bestandt. des AMs, Überempfindlichkeitsreaktionen (z. B. Bronchospasmus, Asthma, Rhinitis, Angioödem, Urtikaria) nach der Einnahme von Acetylsalicylsäure od. and. nicht-steroidalen Entzündungshemmern (NSARs) in der Anamnese, ungeklärte Blutbildungsstör., bestehende od. in der Vergangenheit wiederholt aufgetretene peptische Ulcera od. Hämorraghien (mind. 2 unterschiedl. Episoden nachgewiesener Ulceration od. Blutung), gastrointestinale Blutungen od. Perforation in der Anamnese im Zusammenhang mit einer vorherigen Therapie mit NSAR, zerebrovaskuläre od. and. aktive Blutungen, schwere Leber- od. Nierenfunktionsstör., schwere Herzinsuff. (NYHA-Klasse IV), schwere Dehydratation (verursacht durch Erbrechen, Diarrhoe od. unzureichende Flüssigkeitsaufnahme), letztes Drittel der Schwangerschaft. Kdr. unter 20 kg KG od. unter 6 J. Warnhinw.: AM enth. weniger als 1 mmol (23 mg) Natrium pro Filmtbl. Schwangerschaft/Stillzeit: Währ. des ersten und zweiten Schwangerschaftstrimenons nur geben, wenn unbedingt erforderl., im dritten Trimenon kontraind. Bei kurzfristiger Anw. Stillen mögl. Nebenwirkungen: Peptische Ulcera, Perforationen, gastrointestinale Blutungen, Übelkeit, Erbrechen, Diarrhoe, Flatulenz, Verstopfung, Dyspepsie, Bauchschmerzen, Teerstuhl, Hämatemesis, ulzerative Stomatitis, Verschlimmerung von Colitis und Morbus Crohn, Gastritis, Ödeme, Bluthochdruck, Herzinsuff., geringfügig erhöhtes Risiko arterieller thrombotischer Ereignisse (z. B. Myokardinfarkt od. Schlaganfall). Verschlechterung infektionsbedingter Entzünd. (z. B. Entwickl. einer nekrotisierenden Fasciitis), Symptomatik einer aseptischen Meningitis mit Nackensteifigkeit, Kopfschmerzen, Übelkeit, Erbrechen, Fieber od. Bewusstseinstrübung. Stör. der Blutbildung (Anämie, Leukopenie, Thrombozytopenie, Panzytopenie, Agranulozytose). Überempfindlichkeitsreaktionen mit Hautausschlag und Juckreiz sowie Asthmaanfälle (ggf. mit Blutdruckabfall), schwere allg. Überempfindlichkeitsreaktionen, sie können sich äußern als Gesichtsödem, Zungenschwellung, innere Kehlkopfschwellung mit Einengung der Luftwege, Atemnot, Herzjagen, Blutdruckabfall bis hin zum bedrohl. Schock. Psychotische Reaktionen, Depression. Zentralnervöse Stör. wie Kopfschmerzen, Schwindel, Schlaflosigkeit, Erregung, Reizbarkeit, Müdigkeit. Sehstör. Tinnitus. Palpitationen, Herzinsuff., Herzinfarkt. Arterielle Hypertonie. Gastrointestinale Beschwerden wie Sodbrennen, Bauchschmerzen, und geringfügige Magen-Darm-Blutverluste, die in Ausnahmefällen eine Anämie verursachen können, gastrointestinale Ulzera, u. U. mit Blutung und Perforation, Ösophagitis, Pankreatitis, Ausbildung intestinaler, diaphragmaartiger Strikturen. Leberfunktionsstör., Leberschäden, insbes. bei Langzeittherapie, Leberversagen, akute Hepatitis. Hautausschläge unterschiedl. Art, bullöse Hautreaktionen einschl. Stevens-Johnson-Syndrom und toxische epidermale Nekrolyse (Lyell-Syndrom), Alopezie, schwere Hautinfektionen und Weichteilkomplikationen währ. einer Varizelleninfektion, Arzneimittelexanthem mit Eosinophilie und systemischen Symptomen (DRESS), akute generalisierte exanthematische Pustulose (AGEP), Lichtempfindlichkeitsreaktionen. Papillennekrose, erhöhte Harnsäurekonz. im Blut, vermind. Harnausscheidung, Ödeme, nephrotisches Syndrom; interstitielle Nephritis, die mit einer akuten Niereninsuff. einhergehen kann. Verkehrshinweis! Wechselwirkungen: Nichtsteroidale Antiphlogistika/Antirheumatika einschl. Salicylate. Digoxin, Phenytoin, Lithium. Diuretika, ACE-Hemmer, Betarezeptorenblocker, Angiotensin-II-Antagonisten. Glucocorticoide. Antikoagulanzien. Thombozyten-Aggregationshemmer und SSRI. Acetylsalicylsäure. Methotrexat. Zidovudin. Ciclosporin. Sulfonylharnstoffe. Tacrolimus. Probenecid, Sulfinpyrazon. Chinolon-Antibiotika. CYP2C9-Inhibitoren wie Voriconazol und Fluconazol. Dosierung: Erw.: Initialdosis 200 mg od. 400 mg Ibuprofen. Gesamtdosis von 1200mg Ibuprofen/24 h sollte nicht überschritten werden. Kdr. größer/gleich 20kg KG (ab 6J.) und Jugendl.: 7-10 mg/kg KG als ED bis max. 30 mg/kg KG als Tagesgesamtdosis. Status: Apothekenpflichtig. Stand: 1/21.
Ginkobil® ratiopharm 40 mg Filmtabletten Ginkobil® ratiopharm 80 mg Filmtabletten Ginkobil® ratiopharm 120 mg Filmtabletten Ginkobil® ratiopharm 240 mg Filmtabletten Ginkobil® ratiopharm Tropfen 40 mg Wirkstoff: Ginkgo-biloba-Blätter-Trockenextrakt. Zusammensetzung: -Filmtbl.: 1 Filmtbl. enth. 40 mg, 80 mg; 120 mg; 240 mg quantifizierter, raffinierter Trockenextrakt aus Ginkgobiloba- Blättern (35-67:1), Auszugsmittel: Aceton 60 % (m/m). Der Extrakt ist quantifiziert auf 8,8-10,8 mg; 17,6-21,6 mg; 26,4-32,4 mg; 52,8-64,8 mg Flavonoide, ber. als Flavonoidglykoside, 1,12-1,36 mg; 2,24-2,72 mg; 3,36-4,08 mg; 6,72-8,16 mg Ginkgolide A, B, C, 1,04-1,28 mg; 2,08-2,56 mg; 3,12-3,84 mg; 6,24-7,68 mg Bilobalid, u. enth. unter 0,2 μg; 0,4 μg; 0,6 μg; 1,2 μg Ginkgolsäuren pro Filmtbl. -Tropfen: 1 ml Flüssigkeit (entspr. 20 Tr.) enth. 40 mg quantifizierter, raffinierter Trockenextrakt aus Ginkgo-biloba-Blättern (35- 67:1), Auszugsmittel: Aceton 60 % (m/m). Der Extrakt ist quantifiziert auf 8,8-10,8 mg Flavonoide, ber. als Flavonolglykoside, 1,12-1,36 mg Ginkgolide A, B, C, 1,04-1,28 mg Bilobalid, u. enth. unter 0,2 μg Ginkgolsäuren pro 20 Tr. Sonst. Bestandt.: -40 mg; 80 mg; 120 mg Filmtbl.: Croscarmellose-Natrium; Hochdisperses Siliciumdioxid; Hypromellose; Lactose-Monohydrat; Macrogol 1500; Magnesiumstearat (Ph. Eur.); Maisstärke; Mikrokristalline Cellulose; Simeticon-alpha-Hydro-omega-octadecyloxypoly(oxyethylen)-5- Sorbinsäure(Ph. Eur.)-Wasser; Talkum; Titandioxid. -40 mg Filmtbl. zusätzl.: Eisen(III)- hydroxid-oxid x H2O. -80 mg Filmtbl. zusätzl.: Eisen(III)-oxid, Eisenoxide und –hydroxide. - 120 mg Filmtbl. zusätzl.: Eisen(III)-oxid. -240 mg: Croscarmellose-Natrium, Dimeticon 350, Hochdisperses Siliciumdioxid, Hypromellose, Lactose-Monohydrat, Macrogol 1500, Macrogolstearylether-5 (Ph. Eur.), Magnesiumstearat (Ph. Eur.) [pflanzlich], Maisstärke, Mikrokristalline Cellulose, Sorbinsäure (Ph. Eur.), Talkum, Titandioxid; Eisen(III)-oxid. - Tropfen: Glycerol 85 %, Propylenglykol, Saccharin-Natrium 2 H2O, Gereinigtes Wasser. Anwendungsgebiete: -40 mg; 80 mg; 120 mg; Tropfen: Zur symptomatischen Behandl. von hirnorganisch bedingten Leistungsstör. im Rahmen eines therapeut. Gesamtkonzeptes bei dementiellen Syndromen mit der Leitsymptomatik: Gedächtnisstör., Konzentrationsstör., depressive Verstimmung, Schwindel, Ohrensausen, Kopfschmerzen. Zur primären Zielgruppe gehören dementielle Syndrome bei primär degenerativer Demenz, vaskulärer Demenz und Mischformen aus beiden. Verläng. der schmerzfreien Gehstrecke bei peripherer arterieller Verschlusskrankheit bei Stadium II nach FONTAINE (Claudicatio intermittens) im Rahmen physikalisch-therapeut. Maßn., insbes. Gehtraining. Vertigo und Tinnitus (adjuvante Therapie) bei vaskulärer und involutiver Genese. -40 mg; 80 mg; Tropfen zusätzl: Das individuelle Ansprechen auf die Medikation kann nicht vorausgesagt werden. Bevor Behandl. begonnen wird, abklären, ob Krankheitssymptome nicht auf einer spezifisch zu behandelnden Grunderkrankung beruhen. Bei häufig auftretenden Schwindelgefühlen und Ohrensausen Abklärung durch Arzt. Bei plötzl. auftretender Schwerhörigkeit bzw. Hörverlust sofort Arzt aufsuchen. -240 mg: Zur Verbesserung einer altersbed. kognitiven Beeinträchtigung und der Lebensqualität bei leichter Demenz. Gegenanzeigen: Überempfindlichkeit gg. Ginkgo-biloba od. einen der sonst. Bestandt., Schwangerschaft. Warnhinw.: -Filmtbl.: AM enth. Lactose u. weniger als 1 mmol Natrium (23 mg) pro Filmtbl., d.h. es ist nahezu „natriumfrei“. -Tropfen: AM enth. weniger als 1 mmol (23 mg) Natrium pro 40 Tr., d.h., es ist nahezu „natriumfrei“. Nebenwirkungen: -40 mg; 80 mg; 120 mg; Tropfen: Blutungen an einzelnen Organen, allergischer Schock, allergische Hautreaktionen (Hautrötung, Hautschwellung, Juckreiz), leichte Magen-Darm-Beschwerden, Kopfschmerzen, Schwindel, Verstärkung bereits bestehender Schwindelbeschwerden. -240 mg: Blutungen an einzelnen Organen (Auge, Nase, Gehirn, Gastrointestinaltrakt). Kopfschmerzen, Benommenheit/Schwindel. Diarrhoe, Bauchschmerzen, Übelkeit, Erbrechen. Überempfindlichkeitsreakt. (allerg. Schock). Allerg. Hautreaktionen (Erythem, Ödem, Juckreiz). Status: Apothekenpflichtig. Stand: 2/20; 12/20 (- Trpf.).